Водород в химии: подготовка к ЕГЭ (формула, химические и физические свойства, подробное описание и происхождение)
Что такое водород
Водород — самый легкий элемент в периодической таблице Менделеева.
Его атомный номер один. Одноатомная форма водорода составляет около 75% барионной массы, она считается самым распространенным веществом во всей Вселенной. Водородная плазма является основным веществом звезд, кроме компактных.

Водород имеет три изотопа:
- протий (1Н);
- дейтерий (2Н);
- тритий (3Н).
К общей характеристике относятся следующие свойства: не имеет цвета, запаха, вкуса. Двухатомная форма (H2) не токсична, но в сочетании с воздухом (или O2) легко воспламеняется и взрывоопасна. Опасность взрыва проявляется и в присутствии других окисляющих газов, например фтора, хлора.
На Земле водород присутствует в составе молекулярных соединений, например, воды. Его роль в кислотно-щелочных реакциях нельзя недооценивать.
История открытия
Первым среди ученых, кто заметил водород, был великий алхимик и врач Средневековья Теофраст Парацельс. В своих алхимических экспериментах, надеясь найти «философский камень», смешивая металлы с кислотами, Парацельс получил неизвестный доселе горючий газ. Правда, отделить этот газ от воздуха не удалось.
Всего через полтора века после Парацельса французскому химику Лемери удалось выделить водород из воздуха и проверить его горючесть. Правда, Лемери не понимал, что полученный им газ был чистым водородом. В то же время к подобным химическим экспериментам привлекался и русский ученый Ломоносов, но прорыв в изучении водорода совершил английский химик Генри Кавендиш, по праву считающийся первооткрывателем водорода.
В 1766 году Кавендишу удалось получить чистый водород, который он назвал «горючим воздухом». Еще через 20 лет талантливому французскому химику Антуану Лавуазье удалось синтезировать воду и извлечь из нее этот самый «горючий воздух» — водород. И, кстати, именно Лавуазье предложил название водорода: «Hydrogenium», также известный как «водород».
Место в таблице Менделеева
Расположение химических элементов в периодической таблице Менделеева основано на их атомном весе, рассчитанном относительно атомного веса водорода. То есть, другими словами, водород и его атомный вес – это краеугольный камень таблицы Менделеева, точка опоры, на основе которой великий химик создал свою систему. Поэтому неудивительно, что водород занимает почетное первое место в таблице Менделеева.
Кроме того, водород обладает следующими характеристиками:
- Атомная масса водорода равна 1,00795.
- Водород имеет три изотопа, каждый из которых имеет индивидуальные свойства.
- Водород — легкий элемент с низкой плотностью.
- Водород обладает как восстановительными, так и окислительными свойствами.
- Вступая в химические реакции с металлами, водород принимает свой электрон и становится окислителем. Такие соединения называются гидратами.

Строение молекулы
Водород – газ, его молекула состоит из двух атомов.

Так выглядит молекула водорода.
Молекулярный водород, образованный из таких двухатомных молекул, взрывается при зажигании зажженной спички. Когда молекула водорода взрывается, она распадается на атомы, которые становятся ядрами гелия. Так происходят ядерные реакции на Солнце и других звездах: за счет постоянного распада молекул водорода наша звезда обжигает и согревает нас своим теплом.
Нахождение в природе, изучение его свойств
Звездная температура позволяет водороду существовать в виде плазмы. Она составляет около 6000°С. Однако пространство между звездами заполнено отдельными молекулами, атомами и ионами, часто образующими молекулярные скопления различных размеров и форм – облака. Плотность вещества не является постоянной величиной, как и его температура.
В земной коре водород считается десятым по распространенности элементом. Его массовая доля составляет 1%. При этом она достигает 17% по количеству атомов. Это второе место после кислорода, доля которого составляет 52%. Отсюда важная роль водорода в природе, особенно в химических превращениях.
Водород, в отличие от кислорода, не может существовать в свободном состоянии, только в связанном. Исключение составляет атмосфера, в сухом остатке которой находится 0,00005 % простого вещества — водорода.
Все органические вещества содержат водород. Его доля в живых клетках велика (по числу атомов его удельный вес достигает 63%).
В составе воды водород имеет большое значение в ходе геохимических процессов. Поэтому вулканические газы вызывают выделение некоторого количества водорода по разломам (причина — рифтогенез). По этой же причине водород часто встречается в районе угольных месторождений.
Природные минералы могут содержать H2 в виде ионов аммония, гидроксильных ионов и воды.
Причина появления молекул Н2 в атмосфере – разложение формальдегида, участника окисления метана и других органических соединений. Также причиной их образования является неполное сгорание топлива и биомассы, фиксация азота некоторыми микроорганизмами, содержащимися в воздухе.
Молекулы водорода легкие, поэтому они имеют высокую тепловую скорость. Попадая в верхние слои атмосферы, такие молекулы часто улетают в космос, при этом их потери могут достигать 3 кг в секунду.
Химические и физические свойства
Начиная говорить о химических свойствах водорода, необходимо указать на исключительную прочность его двухатомной молекулы. Для того, чтобы он распался и атомы взаимодействовали с другими участниками химической реакции, необходима энергия:
12H2→ 2H-432 кДж
Нормальные температурные условия обеспечивают протекание реакций только с высокоактивными металлами, например, с кальцием:
12Са+Н2 → СаН2
Исключение составляет реакция с фтором, продуктом которой является фтористый водород:
12F2+H2→ 2HF
При возможности повышения температуры (или при других воздействиях, например, при освещении) водород может реагировать с большинством металлов и неметаллов:
12О2+2Н2→ 2Н2О
В реакциях с галогенами образуются галогеноводороды:
12H2+F2→ 2HF (взрыв происходит в темноте)
12H2+Cl2→ 2HCl (происходит легкий взрыв)
При взаимодействии с оксидами водород проявляет восстановительные свойства:
12CuO+H2→ H2O+Cu
Высокая температура позволяет реагировать с сажей:
12С+2Н2→ СН4
Когда активные металлы соединяются с водородом, образуются гидриды, такие как гидрид натрия (NaH), гидрид кальция (CaH2), гидрид магния (MgH2). К таким твердым веществам, подобным солям и легко гидролизующимся, относятся:
12СаН2+2Н2→ Са(ОН)2+2Н2
Оксиды металлов, реагируя с водородом, восстанавливаются с выделением воды:
12Fe2O3+3H2→ 2Fe+3H2O
Благодаря свойствам водорода он нашел применение для восстановления органических веществ. Реакции протекают с участием катализатора, а также при высоких параметрах давления и температуры. Например, насыщенные алканы образуются при гидрировании алкенов и ненасыщенных алкинов.
Физические свойства водорода:
- в 14,5 раз легче воздуха. Поэтому молекулы движутся быстрее других молекул газа, передавая тепло.
- Обладает высокой теплопроводностью (в 7 раз выше, чем у воздуха).
- Двухатомная молекула.
- Плотность — 0,08987 г/л, температура кипения — 252,76°С, удельная теплота сгорания — 120,9*106 Дж/кг, растворимость в воде — 18,8 мл/л
Он хорошо растворяется в металлах, поэтому может диффундировать в них. Нерастворим в серебре.

Электронная схема водорода
Порядок заполнения оболочек атома водорода (H) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6д → 7р.
На подуровне «s» может находиться до 2 электронов, на «s» до 6, на «d» до 10 и на «f» до 14 электронов
Водород имеет 1 электрон, заполните электронные оболочки в порядке, описанном выше:
1 электрон на 1s подуровень
Степень окисления водорода
Атомы водорода в соединениях имеют степени окисления 1, 0, -1.
Степень окисления – это условный заряд атома в соединении: связь в молекуле между атомами основана на обмене электронами, поэтому, если заряд атома виртуально увеличивается, то степень окисления отрицательная (электроны переносят отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Соединения водорода
Основные степени окисления водорода +1, 0, -1.
Типичные соединения водорода:
| Степень окисления | Типичные соединения |
| +1 | кислоты H2SO4, H2S, HCl и др.
вода H2O и другие летучие соединения водорода (HCl, HBr) кислые соли (NaHCO3 и др.) основания NaOH, Cu(OH)2 основные соли (CuOH)2CO3 |
| -один | гидриды металлов NaH, CaH2 и др. |
Вычисление водорода
В химических реакциях, кроме жидких и твердых веществ, участвуют и газы. Расчеты с газообразными веществами обычно производятся в единицах объема 
Равные объемы разных газов при одинаковых условиях содержат одинаковое количество молекул. Например, 22,4 литра любого газообразного вещества при 0°C и давлении 101,325 кПа содержат 
молекулы.
Плотность газа р – это отношение молярной массы газа (М) к его молярному объему

Относительная плотность газов рассчитывается как отношение их молекулярных масс по уравнению:

Вычисление объема газов по уравнениям химических реакций
Пример 1
Какой объем 6,8 г 
в нормальных условиях?
Решение:


набирать объем в нормальных условиях 
— XL.
Решая пропорцию, находим:

Ответ: 4,48 литра.
Пример #2
Какой объем водорода при стандартных условиях выделится при растворении 3,25 г цинка в избытке соляной кислоты?
Решение:
Напишем уравнение реакции и приравняем его:

Составим пропорцию на основе уравнения реакции и решим задачу:

Ответ: 1,12 литра.
Пример №3
Какой объем водорода потребуется для восстановления 28,8 г FeO? Решение:
Напишем уравнение реакции:

Из уравнения реакции видно, что для восстановления 1 моля (72 г) FeO требуется 1 моль (22,4 л) водорода.
Для восстановления 72 г FeO требуется 22,4 литра

Ответ: 8,96 литра.
Пример №4
Для получения кислорода в лаборатории используют термическое разложение бертолетовой соли. Какой объем кислорода и сколько KS1 образуется из 4,9 г этой соли при стандартных условиях?
Решение:
Запишем уравнение реакции разложения бертолетовой соли 
и приравниваем:

Ответ: 1344 литра 
и 2,98 г KS1.
Расчет объемных отношений газов из химических уравнений
Пример №5
В каком объемном соотношении необходимо взять водород и кислород, чтобы они прореагировали без остатка? Какой объем кислорода вступит в реакцию с 10 л водорода?
Решение:
1) Запишем уравнение реакции взаимодействия кислорода с водородом:

2Н2 + 02 = 2Н20.
Из уравнения известно, что 2 моля водорода без остатка реагируют с 1 молем кислорода.
2 моля водорода занимают объем 44,8 л, а 1 моль кислорода — 22,4 л. Соотношение объемов будет:

Следовательно, водород без остатка реагирует с кислородом в объемных соотношениях, представляющих собой небольшие целые числа — 2:1, т.е. 2 литра водорода без остатка реагируют с 1 литром кислорода.
2) Найдите объем кислорода, вступившего в реакцию с 10 л водорода. 1 литр кислорода взаимодействует с 2 литрами водорода,
от 10 л — xlx = 5 литров.
Ответ: 2:1; 5л
Расчет абсолютной и относительной плотности газов
Пример №6
Рассчитайте абсолютную плотность фтористого водорода и его относительную плотность по отношению к водороду.
Решение:
1) Найдите плотность HF.
Молярная масса 1 моль HF равна 20 г, а молярный объем 22,4 л,

2) Найдите относительную плотность HF из

Пример №7
Относительная плотность паров серы по отношению к азоту при комнатной температуре составляет 9,14. Определите формулу паров серы.
Решение:
Определим молярную массу паров серы.

Если относительная молекулярная масса паров серы равна 256, то, разделив ее на относительную атомную массу серы — 32, получим число атомов в молекуле паров серы, т.е. 256 : 32 = 8.
Итак, формула паров серы
Способы получения водорода
Водород представляет собой бесцветный газообразный элемент без запаха с плотностью 1/14 по отношению к воздуху. В свободном виде встречается редко. Обычно водород сочетается с другими химическими элементами: кислородом, углеродом.
Производство водорода для промышленных и энергетических нужд осуществляется различными способами. Наиболее популярны:
- электролиз воды;
- метод концентрации;
- низкотемпературная конденсация;
- адсорбция.
Водород можно выделить не только из газовых соединений или воды. Водород получают путем воздействия высоких температур на древесину и древесный уголь, а также путем переработки биоотходов.

Атомарный водород для производства энергии получают методом термической диссоциации молекулярного вещества в платиновой, вольфрамовой или палладиевой проволоке. Его нагревают в водородной среде при давлении менее 1,33 Па. Для получения водорода используют и радиоактивные элементы.
Электролиз воды
Самый простой и популярный способ извлечения водорода — электролиз воды. Это позволяет получать практически чистый водород. Другими преимуществами этого метода являются:
Принцип работы электролизного генератора водорода:
- доступность сырья;
- получение элемента давления;
- возможность автоматизации процесса за счет отсутствия движущихся частей.
Процедура расщепления жидкости электролизом обратна сжиганию водорода. Суть его в том, что под действием постоянного тока на электродах, погруженных в водный раствор электролита, выделяется кислород и водород.
Дополнительным преимуществом является производство побочных продуктов промышленной ценности. Поэтому кислород в больших объемах необходим для катализа технологических процессов в энергетике, очистки почв и водоемов, утилизации бытовых отходов. Тяжелая вода, полученная электролизом, используется в энергетике в ядерных реакторах.
Получение водорода концентрированием
Этот метод основан на выделении элемента из содержащих его газовых смесей. Таким образом, большая часть вещества, производимого в промышленных объемах, извлекается путем паровой конверсии метана. Водород, полученный в этом процессе, используется в энергетике, нефтепереработке, ракетостроении, а также для производства азотных удобрений. Процесс получения Н2 осуществляется разными способами:
- короткий цикл;
- криогенный;
- мембрана.
Последний метод считается наиболее эффективным и наименее затратным.
Конденсация под действием низких температур
Этот метод получения H2 заключается в сильном охлаждении газообразных соединений под давлением. В результате они превращаются в двухфазную систему, которая впоследствии разделяется сепаратором на жидкую составляющую и газ. Жидкие среды используются для охлаждения:
- вода;
- сжиженный этан или пропан;
- жидкий аммиак.
Эта процедура не так проста, как кажется. Невозможно сразу чисто отделить углеводородные газы. Часть компонентов будет выходить с отбираемым из сепарационного отсека газом, что неэкономично. Проблему можно решить путем глубокого охлаждения сырья перед сепарацией. Но это требует много энергии.
В современных низкотемпературных конденсаторных системах дополнительно предусмотрены колонны деметанизации или деэтанизации. Газовая фаза удаляется с последней ступени разделения, а жидкость после теплообмена направляется в дистилляционную колонну вместе с потоком сырого газа.
Способ адсорбции
При адсорбции для выделения водорода используют адсорбенты — твердые вещества, поглощающие необходимые компоненты газовой смеси. В качестве адсорбентов используются активированный уголь, силикатный гель и цеолиты. Для осуществления этого процесса используются специальные устройства – циклические адсорбенты или молекулярные сита. При реализации под давлением этот метод может восстановить 85 процентов водорода.
Сравнивая адсорбцию с низкотемпературной конденсацией, можно отметить снижение материальных и эксплуатационных затрат на процесс в среднем на 30 процентов. Адсорбционный метод производит водород для получения энергии и с использованием растворителей. Этот метод позволяет извлекать из газовой смеси 90% Н2 и получать конечный продукт с концентрацией водорода до 99,9%.
Добыча водорода в условиях домашнего хозяйства
Методы получения высокотемпературного водорода в домашних условиях неприменимы. Здесь чаще всего используется электролиз воды.
Чтобы получить водород дома, нужен специальный аппарат – электролизер. Вариантов такого оборудования на рынке множество, устройства предлагают как известные технологические корпорации, так и небольшие производители. Фирменные агрегаты стоят дороже, но и качество сборки у них выше.
Прибор имеет небольшой размер и удобен в использовании. Его основные детали:
- реформатор;
- система очистки;
- топливные элементы;
- компрессорное оборудование;
- резервуар для хранения водорода.
В качестве сырья берется простая водопроводная вода, а электричество поступает из обычной розетки. Солнечные батареи экономят электроэнергию.
«Бытовой» водород используется в системах отопления или приготовления пищи. Они также обогащают топливно-воздушную смесь для увеличения мощности автомобильных двигателей.
Еще дешевле сделать устройство самостоятельно в домашних условиях. Сухой элемент представляет собой герметичный контейнер, состоящий из двух электродных пластин в емкости с раствором электролита. Всемирная паутина предлагает множество схем сборки устройств разных моделей:
- с двумя фильтрами;
- с верхним или нижним расположением контейнера;
- с двумя или тремя клапанами;
- с оцинкованной доской;
- на электродах.
Простое устройство для получения водорода создать несложно. Потребуется:
- лезвие из нержавеющей стали;
- прозрачная трубка;
- фурнитура;
- пластиковый контейнер (1,5 л);
- водяной фильтр и обратный клапан.
Кроме того, понадобятся различные метизы: гайки, шайбы, болты. В первую очередь нужно разрезать лист на 16 квадратных отсеков, у каждого из них срезать по одному уголку. В противоположном углу требуется просверлить отверстие для прикручивания пластин. Для обеспечения постоянного тока пластины должны быть соединены по схеме: плюс-минус-плюс-минус. Эти детали изолированы друг от друга трубкой, а в месте соединения болтом и шайбами (три штуки между пластинами). На плюс и минус ставится 8 пластин.
При правильном монтаже края пластин не будут касаться электродов. Собранные части опускают в пластиковый контейнер. В месте соприкосновения стен делаются два крепежных отверстия с помощью болтов. Установите предохранительный клапан для удаления избыточного газа. Фурнитура крепится на крышку контейнера, а швы герметизируются силиконом.
Чтобы протестировать устройство, выполните несколько действий:
- Залейте жидкость.
- Накрыв колпачком, один конец трубки подсоедините к штуцеру.
- Второй опустите в воду.
- Подключитесь к источнику питания.
После подключения устройства к розетке через несколько секунд будет заметен процесс электролиза и осаждения.
Чистая вода не обладает хорошей электропроводностью. Для улучшения этого показателя нужно создать раствор электролита путем добавления щелочи – гидроксида натрия. Он есть в таких составах для прочистки труб, как «Крот».
Практическое применение
Поскольку водород в 14 раз легче воздуха, в старину им наполняли воздушные шары и дирижабли. Но после серии авиакатастроф конструкторам пришлось искать замену водороду (помните, чистый водород — взрывоопасное вещество, и малейшей искры было достаточно, чтобы вызвать взрыв).

Взрыв дирижабля Гинденбург в 1937 году, причиной взрыва стало возгорание водорода (из-за короткого замыкания), на котором летел этот огромный дирижабль.
Поэтому для таких самолетов вместо водорода стали использовать гелий, который к тому же легче воздуха, получение гелия более трудоемко, но он не такой взрывоопасный, как водород.
Однако водород оказался очень хорошим компонентом ракетного топлива. А автомобили, работающие на водородном топливе, более экологичны, чем их дизельные и бензиновые аналоги.
Водород также используется для очистки различных видов топлива, особенно на основе нефти и производных.
Существующие установки
Спрос на водород растет из-за перехода на более чистые и легкие нефтяные топлива, а нефтяное сырье становится все тяжелее. В этом смысле сложно представить современный НПЗ без установки по производству водорода. ДПВ может отсутствовать только в составе НПЗ, работающих по профилю первичной переработки нефти. Стоит отметить, что для производств с развитой архитектурой вторичных процессов ресурсов одного ПЛК может быть недостаточно.









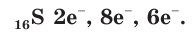



Комментарии 0